Đề thi giữa kì 2 Hóa 10 - Cánh diều - Đề số 7
Số oxi hóa của các nguyên tử trong đơn chất bằng
Đề bài
Số oxi hóa của các nguyên tử trong đơn chất bằng
-
A.
+1
-
B.
-2
-
C.
0
-
D.
+2
Phản ứng nào sau đây là phản ứng oxi hóa – khử?
-
A.
2HCl + FeO \( \to \) FeCl2 + H2O
-
B.
2H2 + O2 \( \to \) 2H2O
-
C.
2Fe(OH)3 \( \to \) Fe2O3 + 3H2O
-
D.
NaCl + AgNO3 \( \to \) AgCl + NaNO3
Quá trình Ostawald để sản xuất nitric acid từ ammonia được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hóa với oxygen ở nhiệt độ cao khi có chất xúc tác:
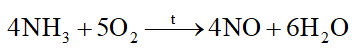
Chất bị oxi hóa trong quá trình trên là
-
A.
NH3
-
B.
O2
-
C.
NO
-
D.
H2O
Dấu hiệu để nhận biết một phản ứng oxi hóa khử là
-
A.
phản ứng có xuất hiện chất khí là chất sản phẩm
-
B.
phản ứng có sự xuất hiện của chất kết tủa
-
C.
phản ứng có sự thay đổi trạng thái của chất phản ứng
-
D.
phản ứng có sự thay đổi số oxi hóa của nguyên tố
Cho phương trình nhiệt hóa học sau: S(s) + O2(g) \( \to \) SO2(g) \({\Delta _r}H_{298}^o = - 296.80kJ\)
Enthalpy tạo thành chuẩn của SO2(g) là
-
A.
-593,60 kJ
-
B.
296,80 kJ
-
C.
-298,80 kJ
-
D.
0,00 kJ
Phản ứng thu nhiệt có
-
A.
\({\Delta _r}H_{298}^o = 0\)
-
B.
\({\Delta _r}H_{298}^o > 0\)
-
C.
\({\Delta _r}H_{298}^o < 0\)
-
D.
\({\Delta _r}H_{298}^o \ne 0\)
Cho 2 phương trình nhiệt hóa học sau:
C(s) + H2O(g) \( \to \) CO(g) + H2(g) \({\Delta _r}H_{298}^o = 121,25kJ\) (1)
CuSO4(aq) + Zn(s) \( \to \) ZnSO4(aq) + Cu(s) \({\Delta _r}H_{298}^o = - 230,04kJ\)(2)
Chọn phát biểu đúng:
-
A.
phản ứng (1) là phản ứng tỏa nhiệt, phản ứng (2) là phản ứng thu nhiệt
-
B.
phản ứng (1) và (2) là phản ứng thu nhiệt
-
C.
phản ứng (1) và (2) là phản ứng tỏa nhiệt
-
D.
phản ứng (1) là phản ứng thu nhiệt, phản ứng (2) là phản ứng tỏa nhiệt
Cho phương trình nhiệt hóa học của phản ứng
2H2(g) + O2(g) \( \to \) 2H2O(l) \({\Delta _r}H_{298}^o = - 571,68kJ\)
Phản ứng trên là phản ứng
-
A.
thu nhiệt và hấp thu 571,68 kJ nhiệt
-
B.
không có sự thay đổi năng lượng
-
C.
tỏa nhiệt và giải phóng 571,68 kJ nhiệt
-
D.
Có sự hấp thụ nhiệt lượng từ môi trường xung quanh
Trong các phản ứng sau, phản ứng không phải là phản ứng oxi hóa – khử?
-
A.
CH4 + 2O2 \( \to \) CO2 + 2H2O
-
B.
Fe + 2HCl \( \to \) FeCl2 + H2
-
C.
BaCl2 + H2SO4 \( \to \) BaSO4 + 2HCl
-
D.
Zn + CuSO4 \( \to \) ZnSO4 + Cu
Số oxi hóa của sulfur (S) trong các phân tử H2SO3, S, SO3, H2S lần lượt là
-
A.
+4, -8, +6, -2
-
B.
+6, +8, +6, -2
-
C.
+4, 0, +6, -2
-
D.
+4, 0, +4, -2
Cho phương trình hóa học của các phản ứng sau:
(a) 2KMnO4 \( \to \) K2MnO4 + MnO2 + O2
(b) Cl2 + 2KOH \( \to \) KCl + KClO + H2O
(c) NH4Cl + NaOH \( \to \) NH3 + NaCl + H2O
(d) CaCO3 \( \to \) CaO + CO2
(e) HCl + NaHCO3 \( \to \) NaCl + CO2 + H2O
(g) 2SO2 + O2 \( \to \) 2SO3
Số phản ứng có kèm theo sự thay đổi số oxi hóa của các nguyên tử là
-
A.
6
-
B.
3
-
C.
5
-
D.
4
Cho nhiệt tạo thành chuẩn của các chất tương ứng trong phương trình

Biến thiên enthalpy của phản ứng N2O4(g) + 3CO(g) \( \to \) N2O(g) + 3CO2(g) có giá trị là:
-
A.
-209,66 kJ
-
B.
-776,11 kJ
-
C.
776,11 kJ
-
D.
210,11 kJ
Những ngày nóng nực, pha viên vitamin C vào nước để giải khát, khi viên sủi tan, thấy nước trong cốc mát hơn là do
-
A.
xảy ra phản ứng tỏa nhiệt
-
B.
xảy ra phản ứng thu nhiệt
-
C.
xảy ra phản ứng trao đổi chất với môi trường
-
D.
có sự giải phóng nhiệt lượng ra ngoài môi trường
Enthalpy tạo thành chuẩn của một đơn chất bền là
-
A.
biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với hydrogen
-
B.
là biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với oxygen
-
C.
bằng 0
-
D.
được xác định từ nhiệt độ nóng chảy của nguyên tố đó
Cho các phản ứng sau xảy ra ở điều kiện chuẩn
CH4(g) + 2O2 \( \to \) CO2(g) + 2H2O (l) \({\Delta _r}H_{298}^o = - 890,36kJ\)
CaCO3(g) \( \to \) CaO(s) + CO2(g) \({\Delta _r}H_{298}^o = 178,29kJ\)
Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn m gam CH4(g) để cung cấp nhiệt tạo cho phản ứng tạo 3 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%. Giá trị gần nhất của m là
-
A.
9,6 gam
-
B.
6,4 gam
-
C.
3,2 gam
-
D.
4,8 gam
Dựa vào phươgn trình nhiệt hóa học của phản ứng sau:
H2(g) + F2(g) \( \to \) 2HF(g) \({\Delta _r}H_{298}^o = - 546,00kJ\)
Giá trị \({\Delta _r}H_{298}^o\)của phản ứng \(\frac{1}{2}{H_2}(g) + \frac{1}{2}{F_2}(g) \to HF(g)\)là
-
A.
-546 kJ
-
B.
546 kJ
-
C.
-273 kJ
-
D.
273 kJ
Bình “gas” sử dụng trong hộ gia đình A có chứa 10,76 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 3:7 (thành phần khác không đáng kể). Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Hỏi trung bình lượng nhiệt tiêu thụ từ đốt 1 bình khí “gas” trên của hộ gia đình A tương ứng với bao nhiêu số điện? (Biết hiệu suất sử dụng nhiệt là 67% và 1 số điện = 1 kWh = 3600 kJ).
-
A.
89 số.
-
B.
97 số.
-
C.
101 số.
-
D.
99 số.
Theo nghiên cứu của Đại học Harvard vào năm 2013, trẻ em sinh sống tại những khu vực có nguồn nước bị nhiễm Fluorine có chỉ số IQ trung bình sẽ thấp hơn so với những trẻ em sống tại vùng khác. Anion F- (fluoride) có độc tính mạnh với hệ thần kinh. Với lượng tương đối thấp: 0,2 gam ion Ftrên cơ thể có trọng lượng 70 kg có thể gây tử vong. Tuy nhiên, sự có mặt của anion fluoride lại giúp men răng chắc khỏe và chống chọi các bệnh về sâu răng, vì vậy anion fluoride được thêm vào nước uống đóng chai với nồng độ 1mg ion Ftrên 1L nước và bổ sung một lượng nhỏ dưới dạng muối sodium fluoride (NaF) trong kem đánh răng. 1. Một bạn học sinh nặng khoảng 63kg sử dụng loại nước chứa ion Fvới lượng 1mg/1L để giúp men răng chắc khỏe, chống sâu răng. Sau khi đọc thông tin về độc tính của ion F- , bạn học sinh rất lo lắng. Hãy tính xem với thể tích nước mà bạn học sinh này uống một ngày là bao nhiêu lít thì ion Fcó trong nước đạt đến mức có thể gây độc tính?
-
A.
160 lít.
-
B.
180 lít.
-
C.
200 lít.
-
D.
170 lít
Theo hiệp hội nha khoa Hoa Kỳ, một người trưởng thành nên bổ sung 3,0 mg F- mỗi ngày dưới dạng muối sodium fluoride (NaF) để ngăn ngừa sâu răng. Lượng NaF không gây độc cho cơ thể khi ở mức 3,19.10-2 gam/ 1 kg cơ thể. Một mẫu kem đánh răng chứa 0,28% NaF, hãy tính khối lượng mẫu kem đánh răng mà một người nặng 65 kg có thể nuốt nhưng không gây độc tính với cơ thể?
-
A.
739,56 gam.
-
B.
789,34 gam.
-
C.
740,53 gam.
-
D.
750,29 gam
Lời giải và đáp án
Số oxi hóa của các nguyên tử trong đơn chất bằng
-
A.
+1
-
B.
-2
-
C.
0
-
D.
+2
Đáp án : C
Số oxi hóa một số chất
Số oxi hóa của các nguyên tử trong đơn chất bằng 0.
Đáp án C
Phản ứng nào sau đây là phản ứng oxi hóa – khử?
-
A.
2HCl + FeO \( \to \) FeCl2 + H2O
-
B.
2H2 + O2 \( \to \) 2H2O
-
C.
2Fe(OH)3 \( \to \) Fe2O3 + 3H2O
-
D.
NaCl + AgNO3 \( \to \) AgCl + NaNO3
Đáp án : B
Phản ứng oxi hóa – khử là những phản ứng có sự thay đổi số oxi hóa
Phản ứng oxi hóa – khử: 2H2 + O2 \( \to \) 2H2O
Đáp án B
Quá trình Ostawald để sản xuất nitric acid từ ammonia được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hóa với oxygen ở nhiệt độ cao khi có chất xúc tác:
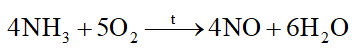
Chất bị oxi hóa trong quá trình trên là
-
A.
NH3
-
B.
O2
-
C.
NO
-
D.
H2O
Đáp án : A
Chất khử là chất cho electron và bị oxi hóa
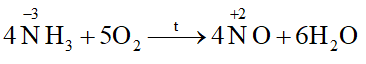
=> NH3 là chất bị oxi hóa
Đáp án A
Dấu hiệu để nhận biết một phản ứng oxi hóa khử là
-
A.
phản ứng có xuất hiện chất khí là chất sản phẩm
-
B.
phản ứng có sự xuất hiện của chất kết tủa
-
C.
phản ứng có sự thay đổi trạng thái của chất phản ứng
-
D.
phản ứng có sự thay đổi số oxi hóa của nguyên tố
Đáp án : D
Dấu hiệu phản ứng oxi hóa – khử
Dấu hiệu để nhận biết một phản ứng oxi hóa khử là phản ứng có sự thay đổi số oxi hóa của nguyên tố
Đáp án D
Cho phương trình nhiệt hóa học sau: S(s) + O2(g) \( \to \) SO2(g) \({\Delta _r}H_{298}^o = - 296.80kJ\)
Enthalpy tạo thành chuẩn của SO2(g) là
-
A.
-593,60 kJ
-
B.
296,80 kJ
-
C.
-298,80 kJ
-
D.
0,00 kJ
Đáp án : C
Biến thiên enthalpy của phản ứng: \({\Delta _r}H_{298}^o = {\Delta _f}H_{298}^o(c{\rm{d}}) - {\Delta _f}H_{298}^o(sp)\)
\({\Delta _r}H_{298}^o = {\Delta _f}H_{298}^o(S{O_2}) = - 296,8kJ/mol\)
Đáp án C
Phản ứng thu nhiệt có
-
A.
\({\Delta _r}H_{298}^o = 0\)
-
B.
\({\Delta _r}H_{298}^o > 0\)
-
C.
\({\Delta _r}H_{298}^o < 0\)
-
D.
\({\Delta _r}H_{298}^o \ne 0\)
Đáp án : B
Đặc điểm phản ứng nhiệt hóa học
Phản ứng thu nhiệt có \({\Delta _r}H_{298}^o > 0\)
Đáp án B
Cho 2 phương trình nhiệt hóa học sau:
C(s) + H2O(g) \( \to \) CO(g) + H2(g) \({\Delta _r}H_{298}^o = 121,25kJ\) (1)
CuSO4(aq) + Zn(s) \( \to \) ZnSO4(aq) + Cu(s) \({\Delta _r}H_{298}^o = - 230,04kJ\)(2)
Chọn phát biểu đúng:
-
A.
phản ứng (1) là phản ứng tỏa nhiệt, phản ứng (2) là phản ứng thu nhiệt
-
B.
phản ứng (1) và (2) là phản ứng thu nhiệt
-
C.
phản ứng (1) và (2) là phản ứng tỏa nhiệt
-
D.
phản ứng (1) là phản ứng thu nhiệt, phản ứng (2) là phản ứng tỏa nhiệt
Đáp án : D
Giá trị biến thiên enthalpy của phản ứng thu nhiệt, phản ứng tỏa nhiệt
Phản ứng (1) \({\Delta _r}H_{298}^o = 121,25kJ\)> 0 \( \to \) phản ứng thu nhiệt
Phản ứng (2) \({\Delta _r}H_{298}^o = - 230,04kJ\)< 0 \( \to \) phản ứng tỏa nhiệt
Đáp án D
Cho phương trình nhiệt hóa học của phản ứng
2H2(g) + O2(g) \( \to \) 2H2O(l) \({\Delta _r}H_{298}^o = - 571,68kJ\)
Phản ứng trên là phản ứng
-
A.
thu nhiệt và hấp thu 571,68 kJ nhiệt
-
B.
không có sự thay đổi năng lượng
-
C.
tỏa nhiệt và giải phóng 571,68 kJ nhiệt
-
D.
Có sự hấp thụ nhiệt lượng từ môi trường xung quanh
Đáp án : C
Dựa vào lý thuyết về năng lượng hóa học
Phản ứng trên là phản ứng là phản ứng tỏa nhiệt và giải phóng 571,68 kJ nhiệt
Đáp án C
Trong các phản ứng sau, phản ứng không phải là phản ứng oxi hóa – khử?
-
A.
CH4 + 2O2 \( \to \) CO2 + 2H2O
-
B.
Fe + 2HCl \( \to \) FeCl2 + H2
-
C.
BaCl2 + H2SO4 \( \to \) BaSO4 + 2HCl
-
D.
Zn + CuSO4 \( \to \) ZnSO4 + Cu
Đáp án : C
Phản ứng oxi hóa – khử
BaCl2 + H2SO4 \( \to \) BaSO4 + 2HCl \( \to \) Phản ứng trao đổi
Đáp án C
Số oxi hóa của sulfur (S) trong các phân tử H2SO3, S, SO3, H2S lần lượt là
-
A.
+4, -8, +6, -2
-
B.
+6, +8, +6, -2
-
C.
+4, 0, +6, -2
-
D.
+4, 0, +4, -2
Đáp án : C
Số oxi hóa của các nguyên tử nguyên tố
Số oxi hóa của sulfur (S) trong các phân tử H2SO3, S, SO3, H2S lần lượt là +4, 0, + 6, -2
Đáp án C
Cho phương trình hóa học của các phản ứng sau:
(a) 2KMnO4 \( \to \) K2MnO4 + MnO2 + O2
(b) Cl2 + 2KOH \( \to \) KCl + KClO + H2O
(c) NH4Cl + NaOH \( \to \) NH3 + NaCl + H2O
(d) CaCO3 \( \to \) CaO + CO2
(e) HCl + NaHCO3 \( \to \) NaCl + CO2 + H2O
(g) 2SO2 + O2 \( \to \) 2SO3
Số phản ứng có kèm theo sự thay đổi số oxi hóa của các nguyên tử là
-
A.
6
-
B.
3
-
C.
5
-
D.
4
Đáp án : B
Dựa vào lý thuyết về phản ứng oxi hóa – khử
(a) \(2K\mathop M\limits^{ + 7} n\mathop {{O_4} \to }\limits^{ - 2} {K_2}\mathop {Mn}\limits^{ + 6} {O_4} + \mathop {Mn}\limits^{ + 4} {O_2} + \mathop {{O_2}}\limits^o \)
(b) \({\mathop {Cl}\limits^o _2} + 2K{\rm{O}}H \to K\mathop C\limits^{ - 1} l + K\mathop C\limits^{ + 1} lO + {H_2}{\rm{O}}\)
(g) \(\mathop {2S}\limits^{ + 4} {O_2} + {\mathop O\limits^o _2} \to 2\mathop S\limits^{ + 6} {\mathop O\limits^{ - 2} _3}\)
Đáp án B
Cho nhiệt tạo thành chuẩn của các chất tương ứng trong phương trình

Biến thiên enthalpy của phản ứng N2O4(g) + 3CO(g) \( \to \) N2O(g) + 3CO2(g) có giá trị là:
-
A.
-209,66 kJ
-
B.
-776,11 kJ
-
C.
776,11 kJ
-
D.
210,11 kJ
Đáp án : B
Biến thiên enthalpy của phản ứng: \({\Delta _r}H_{298}^o = {\Delta _f}H_{298}^o(c{\rm{d}}) - {\Delta _f}H_{298}^o(sp)\)
\(\begin{array}{l}{\Delta _r}H_{298}^o = {\Delta _f}H_{298}^o({N_2}{\rm{O) + 3}}{\Delta _{\rm{f}}}{\rm{H}}_{298}^o(C{O_2}) - 3{\Delta _f}H_{298}^o(CO) - {\Delta _f}H_{298}^o({N_2}{{\rm{O}}_4})\\ = 82,05 + 3.( - 393,5) - 3.( - 110,5) - 9,16 = - 776,11kJ\end{array}\)
Đáp án B
Những ngày nóng nực, pha viên vitamin C vào nước để giải khát, khi viên sủi tan, thấy nước trong cốc mát hơn là do
-
A.
xảy ra phản ứng tỏa nhiệt
-
B.
xảy ra phản ứng thu nhiệt
-
C.
xảy ra phản ứng trao đổi chất với môi trường
-
D.
có sự giải phóng nhiệt lượng ra ngoài môi trường
Đáp án : B
Một số phản ứng thu nhiệt trong thực tế
Những ngày nóng nực, pha viên vitamin C vào nước để giải khát, khi viên sủi tan, thấy nước trong cốc mát hơn là do xảy ra phản ứng thu nhiệt.
Đáp án B
Enthalpy tạo thành chuẩn của một đơn chất bền là
-
A.
biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với hydrogen
-
B.
là biến thiên enthalpy chuẩn của phản ứng giữa đơn chất đó với oxygen
-
C.
bằng 0
-
D.
được xác định từ nhiệt độ nóng chảy của nguyên tố đó
Đáp án : C
Giá trị biến thiên enthalpu tạo thành chuẩn của một số đơn chất.
Enthalpy tạo thành chuẩn của một đơn chất bền là bằng 0.
Đáp án C
Cho các phản ứng sau xảy ra ở điều kiện chuẩn
CH4(g) + 2O2 \( \to \) CO2(g) + 2H2O (l) \({\Delta _r}H_{298}^o = - 890,36kJ\)
CaCO3(g) \( \to \) CaO(s) + CO2(g) \({\Delta _r}H_{298}^o = 178,29kJ\)
Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn m gam CH4(g) để cung cấp nhiệt tạo cho phản ứng tạo 3 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%. Giá trị gần nhất của m là
-
A.
9,6 gam
-
B.
6,4 gam
-
C.
3,2 gam
-
D.
4,8 gam
Đáp án : A
Tính nhiệt lượng tỏa ra từ các mol chất
Để tạo ra 3 mol CaO(s) \( \to \) Nhiệt lượng cần: 178,29 . 3 = 534,87 KJ
\( \to \) n NH4 = 534,87 : 890,36 = 0,6 mol
\( \to \) m NH4 = 0,6 . 16 = 9,6g
Đáp án A
Dựa vào phươgn trình nhiệt hóa học của phản ứng sau:
H2(g) + F2(g) \( \to \) 2HF(g) \({\Delta _r}H_{298}^o = - 546,00kJ\)
Giá trị \({\Delta _r}H_{298}^o\)của phản ứng \(\frac{1}{2}{H_2}(g) + \frac{1}{2}{F_2}(g) \to HF(g)\)là
-
A.
-546 kJ
-
B.
546 kJ
-
C.
-273 kJ
-
D.
273 kJ
Đáp án : C
Mỗi phương trình có hệ số khác nhau có giá trị biến thiên enthalpy khác nhau
H2(g) + F2(g) \( \to \) 2HF(g) \({\Delta _r}H_{298}^o = - 546,00kJ\)
\(\frac{1}{2}{H_2}(g) + \frac{1}{2}{F_2}(g) \to HF(g)\) \({\Delta _r}H_{298}^o = - 546,00kJ\): 2 = -273 kJ
Đáp án C
Bình “gas” sử dụng trong hộ gia đình A có chứa 10,76 kg khí hóa lỏng (LPG) gồm propane và butane với tỉ lệ mol tương ứng là 3:7 (thành phần khác không đáng kể). Khi được đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Hỏi trung bình lượng nhiệt tiêu thụ từ đốt 1 bình khí “gas” trên của hộ gia đình A tương ứng với bao nhiêu số điện? (Biết hiệu suất sử dụng nhiệt là 67% và 1 số điện = 1 kWh = 3600 kJ).
-
A.
89 số.
-
B.
97 số.
-
C.
101 số.
-
D.
99 số.
Đáp án : D
Phân tích dựa vào dữ kiện đề bài
Gọi số mol của propane và butane lần lượt là 3x, 7x
\( \to \) 44.3x + 58.7x = 10,76.103
\( \to \) x = 20
\( \to \) n C3H8 = 60 mol, n C4H10 = 140 mol
Lượng nhiệt tiêu thụ của hộ gia đình là: (60.2220 + 140.2850).67% = 356574 kJ
\( \to \) Số điện tiêu thụ = 356574 : 3600 = 99 số
Đáp án D
Theo nghiên cứu của Đại học Harvard vào năm 2013, trẻ em sinh sống tại những khu vực có nguồn nước bị nhiễm Fluorine có chỉ số IQ trung bình sẽ thấp hơn so với những trẻ em sống tại vùng khác. Anion F- (fluoride) có độc tính mạnh với hệ thần kinh. Với lượng tương đối thấp: 0,2 gam ion Ftrên cơ thể có trọng lượng 70 kg có thể gây tử vong. Tuy nhiên, sự có mặt của anion fluoride lại giúp men răng chắc khỏe và chống chọi các bệnh về sâu răng, vì vậy anion fluoride được thêm vào nước uống đóng chai với nồng độ 1mg ion Ftrên 1L nước và bổ sung một lượng nhỏ dưới dạng muối sodium fluoride (NaF) trong kem đánh răng. 1. Một bạn học sinh nặng khoảng 63kg sử dụng loại nước chứa ion Fvới lượng 1mg/1L để giúp men răng chắc khỏe, chống sâu răng. Sau khi đọc thông tin về độc tính của ion F- , bạn học sinh rất lo lắng. Hãy tính xem với thể tích nước mà bạn học sinh này uống một ngày là bao nhiêu lít thì ion Fcó trong nước đạt đến mức có thể gây độc tính?
-
A.
160 lít.
-
B.
180 lít.
-
C.
200 lít.
-
D.
170 lít
Đáp án : B
Phân tích dựa vào dữ kiện đề bài
Khối lượng F- gây độc trên cơ thể 63kg = 63.0,2/70 = 0,18 gam Thể tích nước mà bạn học sinh này uống một ngày thì ion F- có trong nước đạt đến mức có thể gây độc tính = 0,18.1000 = 180 lít
Đáp án B
Theo hiệp hội nha khoa Hoa Kỳ, một người trưởng thành nên bổ sung 3,0 mg F- mỗi ngày dưới dạng muối sodium fluoride (NaF) để ngăn ngừa sâu răng. Lượng NaF không gây độc cho cơ thể khi ở mức 3,19.10-2 gam/ 1 kg cơ thể. Một mẫu kem đánh răng chứa 0,28% NaF, hãy tính khối lượng mẫu kem đánh răng mà một người nặng 65 kg có thể nuốt nhưng không gây độc tính với cơ thể?
-
A.
739,56 gam.
-
B.
789,34 gam.
-
C.
740,53 gam.
-
D.
750,29 gam
Đáp án : C
Phân tích dữ kiện đề bài
Khối lượng mẫu kem đánh răng mà một người nặng 65 kg có thể nuốt nhưng không gây độc tính với cơ thể = 3,19.10-2 .65/0,28% = 740,53 gam
Đáp án C
Phát biểu nào sau đây là đúng?
Phản ứng oxi hóa – khử là phản ứng có sự nhường và nhận
Tính số oxi hóa của S trong các hợp chất sau (viết đúng thứ tự hợp chất):
Trong phản ứng oxi hóa – khử, chất nhường electron được gọi là:
Cho dãy gồm các phân tử và ion: Zn, S, FeO, SO2, Fe2+, Cu2+, HCl.
. Số oxi hóa của N trong NH3, HNO2, NO3- lần lượt là:
Số oxi hóa của S trong SO2 và SO42- lần lượt là:










